금할 것인가, 터줄 것인가, 원정시술 논란 줄기세포
덧글 0
|
조회 651
|
2014-03-24 12:53:47
금할 것인가, 터줄 것인가, 원정시술 논란 줄기세포
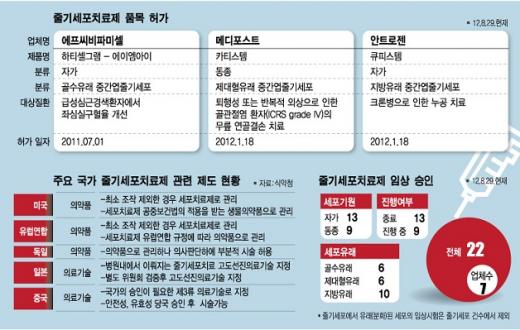
[줄기세포 해외시술 논란]차세대 난치병 치료 희망 vs. 무분별 시술 부작용 우려
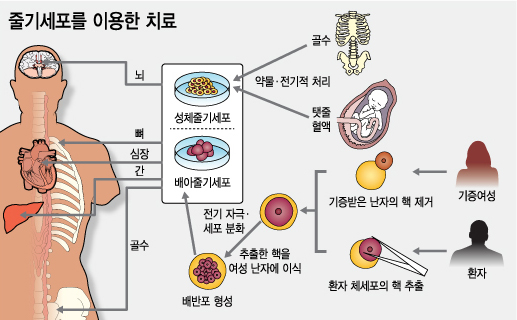
줄기세포가 `차세대 치료법'으로 확산되고 있다. 성형외과에서 미용·건강용으로 시술받거나 희귀난치병이나 중증질환 치료용으로 새삶을 얻었다는 사람들까지 `특효 간증'이 쏟아지고 있다. 그러나 아직 효능과 부작용이 충분히 검증되지 않았으므로 무분별한 시술은 환자의 건강과 재산을 해칠 수 있다는 따가운 비난도 양립한다. 이같은 상황에서 줄기세포업체 중 한 곳인 알앤엘바이오 (278원  100 56.2%)가 해외 원정시술을 해와 논란이 벌어졌다. 지금까지 알앤엘바이오가 해외에서 행한 성체줄기세포 투여횟수는 2만8000회에 달한다. 100 56.2%)가 해외 원정시술을 해와 논란이 벌어졌다. 지금까지 알앤엘바이오가 해외에서 행한 성체줄기세포 투여횟수는 2만8000회에 달한다. ◇국내 줄기세포기술 어디까지= 줄기세포는 기능이 정해지지 않은 원시세포다. 분화를 통해 특정 세포로 변할 수 있다는 게 치료의 근간이다. 초기에는 수정란을 활용하는 배아줄기세포류가 주목받았으나 거듭된 윤리논란, 부작용 문제 등이 커 관심에서 멀어졌고 상업적으로도 퇴색했다. 이를 대체해 최근 성체줄기세포가 각광받고 있다. 지방조직, 골수, 제대혈 등 인체에 산재하며 조직재생을 담당하는 줄기세포다. 환자 몸에서 추출해 배양이 엄격한 환경에서 이뤄지면 이론적으로 치료범위는 제한이 없고 부작용 또한 없다는 평가다. 미국 국립보건원은 줄기세포분야 투자예산의 77%를 성체줄기세포분야에 투자하고 배아줄기세포투자 비율은 12%에 불과하다. 올 2월 현재 국내에서 줄기세포와 관련, 23건의 임상시험이 승인됐는데 배아줄기세포는 단 1건이다. 성체줄기세포는 자기치유능력을 가진 세포를 환자의 몸에서 추출해 활용한다는 점 때문에 중증질환이나 난치병 치료의 희망이 되고 있다. 부작용이 없거나 적고 양산이 가능하다는 잠재력 때문에 세계 각국이 투자에 나서고 있다. 줄기세포치료제의 글로벌시장 규모는 2011년 23억달러에서 2016년까지 84억달러로 연간 12%씩 성장할 것으로 전망된다. 우리나라에서도 상업화되고 있다. 전세계적으로 정식 허가가 난 줄기세포치료제가 4개에 불과한데 이중 3개가 우리나라에서 나왔다. 각각 심근경색환자의 좌심실 펌프기능 개선, 골관절염 환자 무릎 연골치료, 크론병 장 누공 치료에 사용되는 것으로 해당 회사는 파미셀 (4,300원  20 -0.5%), 메디포스트 (81,200원 20 -0.5%), 메디포스트 (81,200원  600 0.7%), 안트로젠이다. 600 0.7%), 안트로젠이다. 김대원 보건산업진흥원 연구원은 "성체줄기세포 중 중간엽줄기세포(MSC)에 대한 연구가 활발한 편"이라며 "여타 성체줄기세포에 비해 증식능력과 분화능력이 우수하며 면역원성의 위험도 적기 때문"이라고 설명했다. 제대혈에서 추출한 줄기세포를 쓰는 메디포스트의 양윤선 대표는 "줄기세포의약품은 아직 초기 단계여서 정식으로 사용 가능한 범위가 매우 좁다"면서도 "기초연구뿐 아니라 이미 수백 개의 줄기세포 의약품들이 세계 각국에서 연구되고 있으며 새로운 기술 융합도 활발히 이뤄지고 있다"고 말했다. 심혈관 줄기세포 분야 국내 최고 권위자인 김효수 서울대병원 순환기내과 교수는 10여년간 심근경색환자를 대상으로 임상치료를 한 결과 줄기세포가 죽은 심근을 살리는 효과가 유의미하게 있음을 확인했다. ◇원정시술 논란 왜? = 그러나 그간 성과에도 불구하고 줄기세포 논란은 계속되고 있고 알앤앨바이오는 국내 절차를 비껴나 해외에서 원정시술을 행하고 있다. 여기에는 사회적 요인이 크게 작용하고 있다. 현행 제도에서 줄기세포를 환자몸에서 추출해 그냥 주입하는 것은 합법이다. 그러나 일단 추출한 것을 `배양'하면 의약품으로 인정돼 시술하려면 일일이 법이 정한 임상시험 절차를 거쳐야 한다. 개별질병에 대해 약품승인이 나기까지 그 긴 시간을 어떻게 기다리느냐는 환자의 다급함이 원정시술 배경으로 작용한다. 규제가 약한 곳에서 `부작용없는 자가치료제'라는 확신을 빨리 확인하고 싶은 알앤엘바이오의 속내도 엿보인다. 초기에는 줄기세포 시술을 원하는 환자들이 알앤엘바이오가 국내에서 배양한 줄기세포치료제를 직접 해외로 들고 나가 시술을 받았다. 하지만 2010년 11월 보건당국이 그것을 금지하자 알앤엘바이오는 줄기세포 배양센터를 중국과 일본으로 이전했다. 알앤엘바이오의 기술이 적용된 배양센터는 일본의 교토와 중국의 베이징에 있다. 줄기세포시술을 받고 싶은 환자가 알앤엘바이오를 찾게 되면 이 회사는 일본이나 중국의 병원을 소개해 준다. 이후 환자는 해당 병원에 의료관련 자료를 보내 시술 가능여부를 우선 확인한다. 시술이 가능하다고 해당 병원 의료진이 판단하면 알앤엘바이오는 환자의 지방에서 줄기세포를 채취한다. 알앤앨바이오는 이 줄기세포를 1차로 배양해 이른바 씨앗줄기세포를 만들어 낸다. 씨앗줄기세포는 대량으로 복제가 되기 전의 줄기세포다. 씨앗줄기세포는 일본이나 중국의 배양센터로 보내져서 대량 배양과정을 거친다. 센터에서 이를 해당 병원으로 보내면 환자는 의료진의 판단 하에 배양된 줄기세포를 투여 받게 된다. 시술이 이뤄진 병원은 일본 후쿠오카의 신주쿠클리닉, 중국 베이징의 연달국제병원, 상하이의 455병원, 연태의 연태해양병원 등이다. 알앤엘바이오 관계자는 "일본과 중국에 있는 배양센터는 알앤엘바이오의 국내 생산시설과 동일한 GMP(우수의약품 제조·관리기준) 생산시설"이라며 "알앤엘바이오의 배양기술도 동일하게 적용됐으며 현지법인의 관리하에 생산이 이뤄지고 있다"고 설명했다. ◇약인가, 시술인가〓 일본이나 중국의 경우 배양된 줄기세포라도 의사가 판단해 환자에게 사용할 수 있는 시술개념으로 분류되고 있다. 미국의 경우 연방법으로는 허가받지 않은 줄기세포 시술을 금지하고 있지만 텍사스 주법으로는 의사가 시술을 할 수 있다. 독일은 줄기세포치료제를 약으로 규정하고 있지만, 정해진 병원에서는 의사의 판단에 따라 시술이 가능하다. 이와 관련 국내논의는 평행선이다. 잠재적 부작용이 충분히 검증되지 않았다는 것이 규제완화에 거부감을 갖게 하고 있다. 논란의 중심에 선 알앤엘바이오는 배양된 성체줄기세포의 잠재력을 활용할 수 있도록 폭넓은 시술을 허용해줄 것을 주장하고 있다. 라정찬 알앤엘바이오 줄기세포기술원장 원장은 머니투데이와의 인터뷰에서 "성체줄기세포 치료영역은 이론적으로 무한하며 임상시험이나 과학적연구를 통해 하나씩 효험이 인정되고 있다"며 "희귀 난치병 환자들이 국내에서 기회를 충분히 갖지 못해 해외로 나가고 있는데, 독일처럼 병원에서 의사책임하에 제한적으로라도 시술을 폭넓게 허용해주는 쪽으로 제도를 고쳐야 한다"고 주장했다. 보건당국과 학계는 줄기세포를 배양할 경우 통상적인 의약품 승인절차를 거쳐야 한다고 강조한다. 한국줄기세포학회는 올 1월 성명을 통해 "줄기세포치료제를 다른 의약품과 마찬가지로 국가적으로 인정된 객관적 검증절차를 거쳐 유효성과 안전성이 확인된 후에 허가돼야할 사항"이라고 밝혔다. 오일환 가톨릭대 의대 교수도 "일부 줄기세포 업체가 제대로 임상시험도 거치지 않은 것을 해외에서 시술하는 것은 큰 문제"라며 " 배양된 줄기세포의 경우 안전성 검증이 반드시 필요한 과정"이라고 지적했다.
|
- 티시바이오주식회사 서울 강남구 테헤란로 145,16층(우신빌딩) | 대표전화 1644-8475 | 대표이사 이상우 | 개인정보관리책임자 김지은
- Copyright © 2017 TC bio 티시바이오 주식회사. All rights reserved.